AL+H2SO4(конц) = .... Дописать уравнения возможных реакций и написать ионное полное и ионное сокращенное
Собственно реакция возможна только одна, и то только при нагревании, так как происходит пассивация алюминия
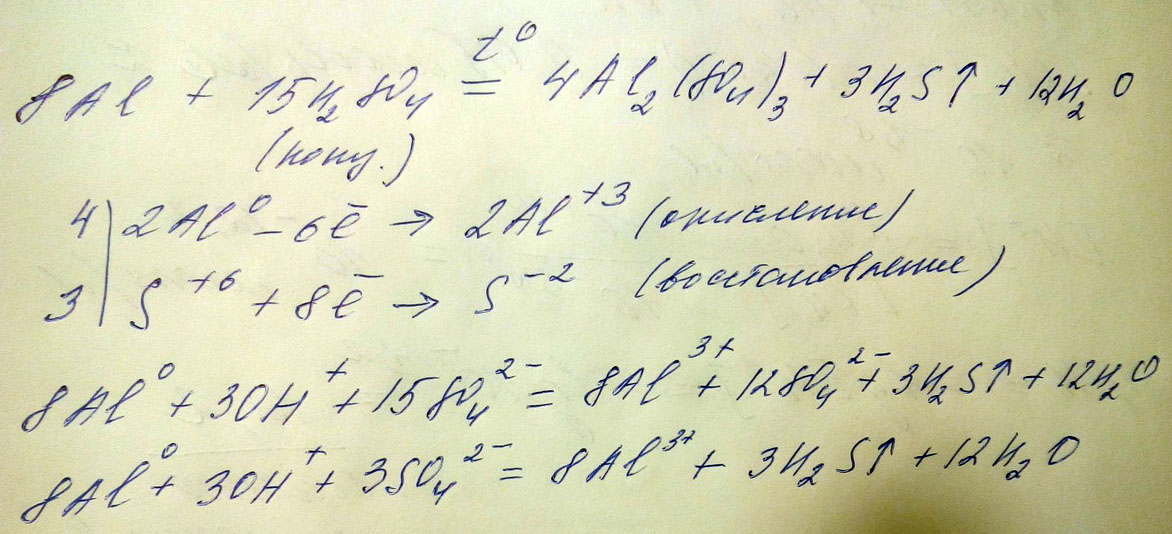
Собственно реакция возможна только одна, и то только при нагревании, так как происходит пассивация алюминия
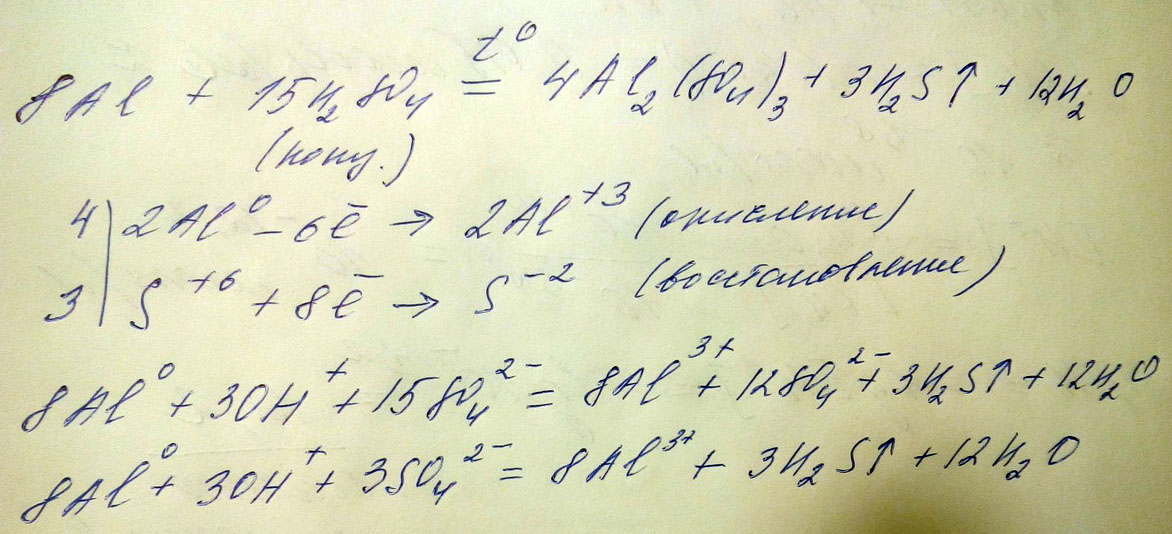
1.2Al2O3+ 9C = Al4C3 + 6CO
2.K2O+CO2(должно быть СО2, если ты не ошиблась то реакции не будет )=K20+CO2 = K2CO3
3.Fe2O3+3Mg = 2Fe+3MgO
4.Na2S+ 2O2 = Na2SO4
5.Na2O+C не идет реакция
6.3MnO2+4Al = 2Al2O3+3Mn
7.ZnO+H2 = ZnO+ H2
8.Na2O+CO2 = Na2CO3
1. CaO + H2O = Ca(OH)2
CO2 + 2KOH = K2CO3 + H2O
2NaOH + H2SO4 = Na2SO4 + 2H2O
2. Щелочи реагируют с кислотными оксидами, солями с признаком реакции (осадок, газ, образование малодиссоциирующего вещества, кислотами.
Из предложенных веществ:
CO2 + 2NaOH = Na2CO3 + H2O (обмен, карбонат натрия
AlCI3 + 3NaOH = AI(OH)3↓ + 3NaCI (обмен, хлорид натрия
H2SiO3 + 2NaOH = Na2SiO3 + 2H2O (обмен, силикат натрия
Реакция с сульфатом калия невозможна, т. к. Не наблюдается признака реакции: K2SO4 + 2NaOH = Na2SO4 + 2KOH
1. CuSO4 + BaCI2 = CuCI2 + BaSO4↓
Cu(2+) + SO4(2-) + Ba(2+) + 2CI(-) = Cu(2+) + 2CI(-) + BaSO4↓
Ba(2+) + SO4(2-) = BaSO4↓
Al(OH)3 + 3HBr = AIBr3 + 3H2O
Al(OH)3 + 3H(+) + 3Br(-) = Al(3+) + 3Br(-) + 3H2O
AI(OH)3 + 3H(+) = AI(3+) + 3H2O
2. 4Li + O2 = 2Li2O
Li2O + H2O = 2LiOH
2LiOH + H2SO4 = Li2SO4 + 2H2O
Li2SO4 + 2HNO3 = 2LiNO3 + H2SO4
CaO+H2O = Ca(OH)2 соединение CO2+2KOH = K2CO3+H2O обмен NaOH+HCl = NaCl+H20 обмен 2) СО2; AlCl3;H2SiO3 CO2+2NaOH= Na2CO3+H2O обмен (соль Na2CO3 - карбонат натрия AlCl3+3NaOH = Al(OH)3+3NaCl обмен (NaCl - хлорид натрия H2SiO3+2NaOH = Na2SiO3+2H2O обмен (Na2SiO3 - силикат натрия
1. 2Al + 6HCl = 2AlCl3 + 3H2
2. 2Ag + 2HCl = 2AgCl (выпадает в осадок + H2
3. 4Zn + 5H2SO4 = 4ZnSO4 + H2S + 4H2O
4. Cu + 2H2SO4 = CuSO4 + SO2 + 2H2O
, что какая-то реакция неосуществима. По этому прописываю все.
Любые металлы реагируют с водой, образуя гидроксиды, варьируется лишь степень их растворимости. Оксиды взаимодействуют с водой в том случае, если образуется растворимое вещество (щелочь, кислота)
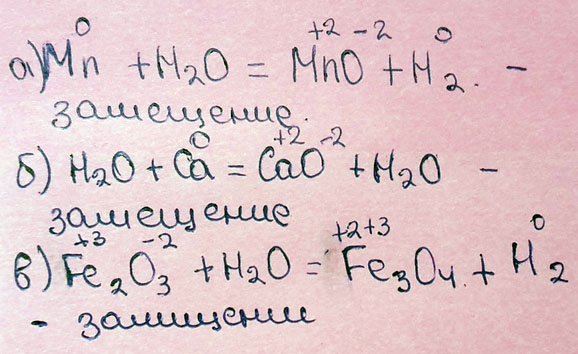
4Li+O2->2Li2O
2Na+H2->2NaH
2K+H2->2KH
2K+2H2O->2KOH+H2
Na2O+H2O->2NaOH
Na2O+SO2->Na2SO3
Седьмой реакции не может быть может вот так:NaOH+HNO3->NaNO3+H2O
2NaOH+CuSO4->Cu(OH)2+Na2SO4
NaOH+CO2->NaHCO3
NaOH+Zn(OH)2->Na2ZnO2+2H2O
1 ВАРИАНТ
1). 2NaOH + H2SO4 = 2H2O + Na2SO4
2). NaOH + SO3 = NaHSO4
3). 2NaOH + CuSO4 =Cu(OH)2 ↓ + Na2SO4
4). NaOH + фенолфталеин = малиновое окрашивание
5). Mg(OH)2 = MgO + H2O
2 ВАРИАНТ
1). КOH + HNO3 = H2O + KNO3
2). 2KOH + N2O5 = 2KNO3 + H2O
3). 2KOH + Cu(NO3)2 =Cu(OH)2↓ + 2KNO3
4). KOH + лакмус = синее окрашивание
5). Pb(OH)2 = PbO + H2O
1. 2HCl+Mg(OH)2 = MgCl2+H2O
Zn+2H2SO4(конц=ZnSO4+H2O+H2S
S+O2 = SO2
H2O+Na2O= 2NaOH
2NaCl+F2= 2NaF
2.Ca+Cl2 = CaCl2 присоединения
2HNO3+Cu(OH)2= 2H2O+ Cu(NO3)2
реакция обмена
2Mg+TiCl4= 2MgCl2+Ti
реакция замещения
2AgBr = 2Ag+Br2
реакция разложения
2Mg+O2 = 2MgO
реакция соединения
6HCl+2Al = 2AlCl3+3H2
реакция замещения
KOH+HCl= H2O+KCl не идёт
Ba(OH)2+H2SO4= BaSO4+4H2O
реакция обмена
2H2O = 2H2+O2
реакция разложения
а. Реакция замещения
б. Реакция соединения
в. Реакция обмена
г. Реакция разложения
2HCI+Mg(OH)2 =MgCl2+H2O(обмен
Zn+H2SO4 = ZnSO4+H2(замещение
S+O2 = SO2(соединение
H2O+Na2O = NaOH(соединение
2NaCl+F2 = 2NaF+2Cl(замещение
а Ca + Cl2 → СaCl2(соединение
б2HNO3 + Cu(OH)2 → Cu(NO3)2 + 2H2O(обмен
в 2Mg + TiCl4 → 2MgCl2+Ti(замещение
г AgBr → Ag+ + Br(разложение
а 2Mg + O2→ 2MgO(соединение
б 2HCl + Al → AlCl2+H2(замещение
в KOH + HCl → KCl+H2O(обмена
г Ba(OH)2 + H2SO4 → BaSO4+H2O(обмена
д 2H2O→ 2H2+O2(соединение
а 2Al + Cr2O3 → Al2O3+2Cr(замещение
б 6Li+N2→2Li3N(соединение
в K2S+CuCl2→CuS↓+2KCl(обмен
г 2N2O→2N2+O2(соединение