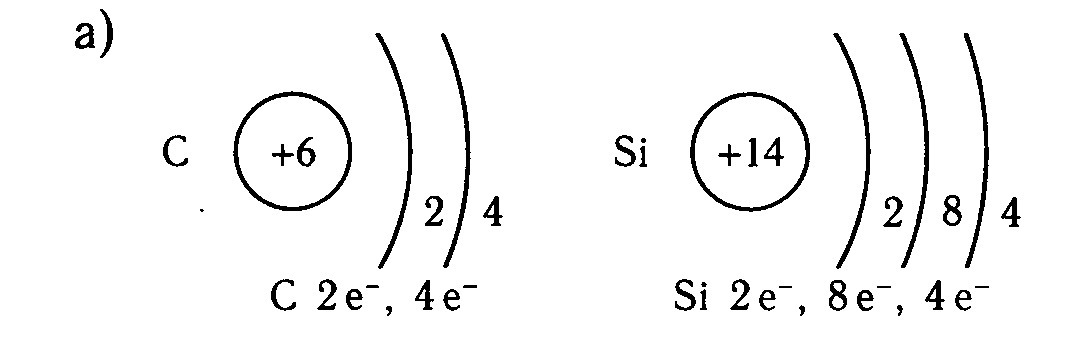Сравните строение и свойства атомов - задачи и примеры
Сравните строение и свойства атомов химических элементов C и Si
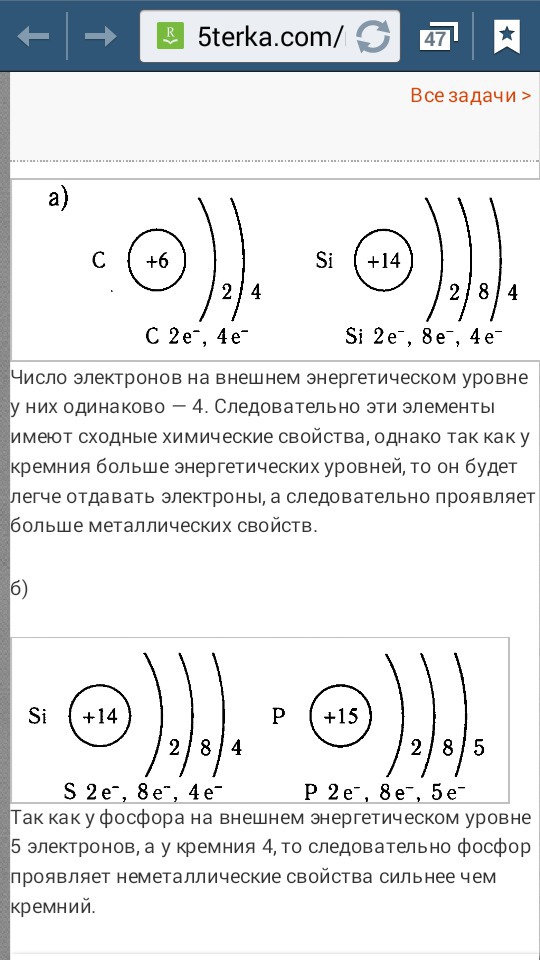
Число электронов на внешнем энергетическом уровне у них одинаково — 4. Следовательно эти элементы имеют сходные химические свойства, однако так как у кремния больше энергетических уровней, то он будет легче отдавать электроны, а следовательно проявляет больше металлических свойств.
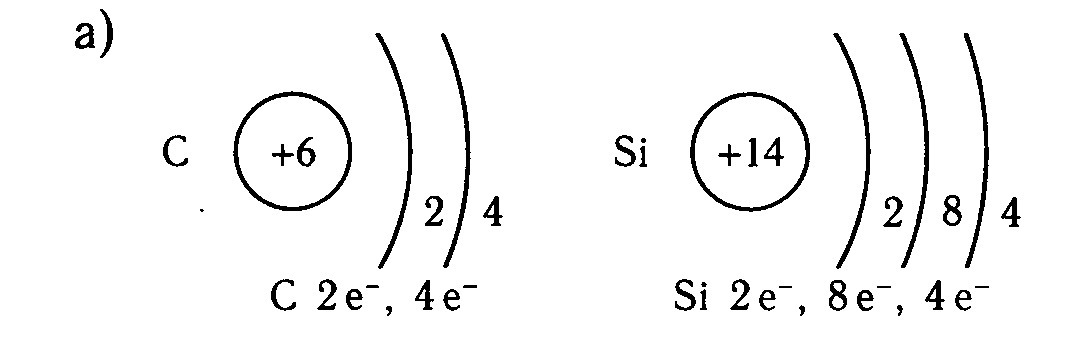
Сравните строение и свойства атомов химических элементов а) C и Si б) Si и P
1) Число электронов на внешнем уровне у углерода и кремния одинаково (4). Заряд ядра у углерода меньше, чем у кремния
1) чем отличается электронное строение и свойства атомов K, Mg, Al от электронного строения и свойств ионов K^+ Mg^2+ Al^3+
2) чем отличается электронное строение и свойства атомов Cl, Br, I от электронного строения и свойств ионов Cl^- Br^- I^-
1. Атом К имеет всего 19 электронов. К^+ имеет 18 электронов, т. к. 1 ē потерял.
Атом Mg имеет 12 ē. Mg^2+ имеет 10 ē.
Атом Al имеет 13 ē. Al^3+ тоже имеет 10 ē.
Ион => образование ионной связи.
Вышеназванные ионы являются катионами, т.к положительно заряжены.
2. Cl имеет 17ē. Cl^- имеет 18ē, т. к. 1 электрон получил.
Br имеет 35ē,Br^- имеет 36ē.
I имеет 53 ē, I^- имеет 54ē.
Вышеназванные ионы являются анионами, т. к. Отрицательно заряжены.
Сравните строение и свойства атомов углерода и кремния, кремния и фосфора
Атом углерода имеет конфигурацию 2s2 2p2
атом кремния 3s2 3p2 то есть кремний находится ниже чем углерод. Последний энергетический уровень у него не второй, а третий, валентные электроны дальше от ядра, металлические свойства у ремния выражены сильней. Чем у углерода. Радиус атома больше
конфигурация фосфора 3s23p3
по сравнению с кремнием у него радиус атома меньше, валентные энергетический уровеньближе к ядру. Окислительные свойства фосфора сильней выражены чем укремния.