Составьте полное и краткое ионное уравнения для 2NO+O2 = 2NO2 и 4NO2+O2+2H2O = 4HNO3
2NO + O2 -> 2NO2
N(+2) -2e -> N(+4) 2 ок-ие
в-ль
O2(0) +4e -> 2O(-2) 1 в-ие
ок-ль
4NO2 + O2 + 2H2O -> 4HNO3
N(+4) -1e -> N(+5) 4 ок-ие
в-ль
O(0) +2e -> O(-2) 2 в-ие
ок-ль
1. Напишите уравнение реакций ионного обмена (в молекулярной, полной ионной и сокращенной ионной формах
1) CuCl2+KOH =
2) Na2CO3+H2SO4
3) Ba(NO3)2+K2SO4 =
4) HCI+NaOH =
5) FeCl3+NaOH =
6) K2CO3+HCl =
7) NaOH+HNO3 =
2. Выберите нерастворимую соль:
1.Cu(OH)2
2.NaCl
3.SrCl2
4.AgCl
CuCl₂ + 2KOH = Cu(OH)₂↓ + 2KCl
Cu²⁺ + 2Cl⁻ + 2K⁺ + 2OH⁻ = Cu(OH)₂↓ + 2K⁺ + 2Cl⁻
Cu²⁺ + 2OH⁻ = Cu(OH)₂↓
Na₂CO₃ + H₂SO₄ = Na₂SO₄ + CO₂↑ + H₂O
2Na⁺ + CO₃²⁻ + 2H⁺ + SO₄²⁻ = 2Na⁺ + SO₄²⁻ + CO₂↑ + H₂O
CO₃²⁻ + 2H⁺ = CO₂↑ + H₂O
FeCl₃ + 3NaOH = Fe(OH)₃↓ + 3NaCl
Fe³⁺ + 3Cl⁻ + 3Na⁺ + 3OH⁻ = Fe(OH)₃↓ + 3Na⁺ + 3Cl⁻
Fe³⁺ + 3OH⁻ = Fe(OH)₃↓
Ba(NO₃)₂ + Na₂SO₄ = 2NaNO₃ + BaSO₄↓
Ba²⁺ + 2NO₃⁻ + 2Na⁺ + SO₄²⁻ = 2Na⁺ + 2NO₃⁻ + BaSO₄↓
Ba²⁺ + SO₄²⁻ = BaSO₄↓
HCl + NaOH = NaCl + H₂O
H⁺ + Cl⁻ + Na⁺ + OH⁻ = Na⁺ + Cl⁻ + H₂O
H⁺ + OH⁻ = H₂O
K₂CO₃ + 2HCl = 2KCl + CO₂↑ + H₂O
2K⁺ + CO₃²⁻ + 2H⁺ + 2Cl⁻ = 2K⁺ + 2Cl⁻ + CO₂↑ + H₂O
CO₃²⁻ + 2H⁺ = CO₂↑ + H₂O
HNO₃ + NaOH = NaNO₃ + H₂O
H⁺ + NO₃⁻ + Na⁺ + OH⁻ = Na.⁺ + NO₃⁻ + H₂O
H⁺ + OH⁻ = H₂O.
нерастворимая соль
Cu(OH)₂
AgCl
1) CuCl2+2KOH->Cu(OH)2↓+2KCL
Cu2+ + 2CL- + 2K+ + 2OH-> Cu(OH)2↓+2K+ +2CL-
Cu2+ + 2OH->Cu(OH)2↓
2) Na2CO3+H2SO4->Na2SO4+H2O+CO2↑
2Na+ + CO3 2- + 2H+ +SO4 2->2Na+ +SO4 2- + H2O + CO2↑
CO3 2-+2H+ -> H2O+CO2↑
3) Ba(NO3)2+K2SO4->BaSO4↓+2KNO3
Ba2+ + 2NO3- + 2K+ + SO4 2->BaSO4 ↓+ 2K+ + 2NO3-
Ba2+ + SO4 2->BaSO4↓
4) HCI+NaOH->NaCL+H2O
H+ +CL- + Na+ + OH->Na+ + Cl- + H2O
H+ + OH->H2O
5) FeCl3+3NaOH->Fe(OH)3↓+3NaCL
Fe3+ + 3Cl- + 3Na+ + 3OH->Fe(OH)3↓+3Na+ + 3CL-
Fe3+ + 3OH-Fe(OH)3↓
6) K2CO3+2HCl->2KCL+H2O+CO2↑
2K+ + CO3 2- + 2H+ + 2Cl->2K+ + 2Cl- + H2O+CO2↑
CO3 2-+ 2H+ ->H2O+CO2↑
7) NaOH+HNO3->NaNO3+H2O
Na+ + OH- + H+ + NO3->Na+ + NO3- + H2O
OH- + H+ ->H2O
2. Выберите нерастворимую соль:
4.AgCl
Дайте характеристику химического элемента Фосфор по плану
-Положение элемента в ПСХЭ
-Строение атома
-Характер простого вещества(металл, неметалл, переходный металл
-сравнение свойств простого вещества со свойствами простых веществ, образованных соседними по подгруппе элемента, соседним по периоду элемента
-Формула оксида и гидроксида, их характер, ответ подтвердите двумя уравнениями химической реакции (Напишите уравнение реакций оксида фосфора (V) и фосфорной кислоты с раствором гидроксида натрия в молекулярном и ионном виде.
1. 3 период V группа главная А подгруппа
2. Заряд ядра +15. Протонов 15, электронов 15, нейтронов 16
2)8)5 р-элемент
3. Неметалл. Имеет несколько аллотропных модификаций-белый, красный, черный, фиолетовый
4. Активнее всех простых веществ своей подгруппы как неметалл.
В периоде более сильный неметалл чем натрий Na, магний Mg алюминий Al, кремний Si. Менее активный как неметалл, чем сера S и хлор Cl
5. Оксид фосфора (V) - P2O5
P2O5+6NaOH = 2Na3PO4+3H2O
гидроксид - фосфорная кислота H3PO4
H3PO4+3NaOH = Na3PO4+3H2O
Напишите уравнение реакций в молекулярном полном ионном и сокрощенном виде между веществами
Хлорид калия и нитратом бария
хлорид бария и сульфат натрия
Азотной кислоты и гидроксидом кальция
Хлорид калия и нитратом бария:
2KCI+ Ba(NO₃)₂⇄ BaCI₂ + 2KNO₃
2K⁺ + 2CI⁻ + Ba²⁺ +2NO₃⁻⇄ Ba²⁺ + 2CI⁻ + 2K⁺ +2 NO₃⁻
хлорид бария и сульфат натрия
BaCI₂+ Na₂SO₄=BaSO₄↓ + 2NaCI
Ba²⁺ + 2CI⁻+ 2Na⁺+SO₄²⁻ = BaSO₄↓ + 2Na⁺ + 2CI⁻
Ba²⁺ +SO₄²⁻ = BaSO₄↓
Азотной кислоты и гидроксидом кальция (может быть два случая:
A) известковое молоко-щелочь
2HNO₃ +Ca(OH)₂=Ca(NO₃)₂ + 2H₂O
2H⁺ + 2NO₃⁻ +Ca²⁺+ 2OH = Ca²⁺ + 2NO₃ + 2H₂O
2H⁺ + 2OH = Ca²⁺ + 2NO₃ + 2H₂O
Б ГИДРОКСИД КАЛЬЦИЯ МАЛОРАСТВОРИМОЕ ВЕЩЕСТВО:
2HNO₃ +Ca(OH)₂=Ca(NO₃)₂ + 2H₂O
2H⁺ + 2NO₃⁻ +Ca(OH)₂ = Ca²⁺ + 2NO₃ + 2H₂O
2H⁺ + Ca(OH)₂= Ca²⁺ + 2H₂O
Напишите уравнение реакций в молекулярной и ионной формах между следующими веществами: а H2SO4 и NaOH б ) HCl и Ca(OH)2; в NaCl и AgNO3; г FeCl3 и NaOH
A) H₂SO₄+2 NaOH =2HOH+Na₂SO₄
2H⁺+ SO₄⁻²+ 2Na⁺+OH⁻ = 2HOH+2Na⁺+SO₄⁻²
2H⁺+OH⁻ = 2HOH
Б2HCl+Ca(OH)₂=2HOH+CaCl₂
2H⁺+2Cl⁻+Ca⁺²+2OH⁻ = 2HOH+Ca⁺²+2Cl⁻
2H⁺+2OH⁻ = 2HOH
в NaCl+AgNO₃=NaNO₃+AgCl
Na⁺+Cl⁻+ Ag⁺+ NO₃⁻= Na⁺+NO₃⁻+ AgCl
Ag⁺+Cl⁻ = AgCl
г FeCl₃+3 NaOH = 3NaCl+ Fe(OH)₃
Fe⁺³+ 3Cl⁻+3Na⁺+3OH⁻ = 3Na⁺+ 3Cl⁻+ Fe(OH)₃
Fe⁺³+3OH⁻= Fe(OH)₃
С какими из нижеперечисленных веществ будет взаимодействовать ортофосфорная кислота, напишите уравнение реакций в молекулярном в ионном виде: 1) гидроксид бария; 2) карбонат натрия; 3) сульфат калия; 4) серебро; 5) нитрат алюминия
Ортофосфорная кислота не вступает в реакцию с сульфатом калия и серебром ...
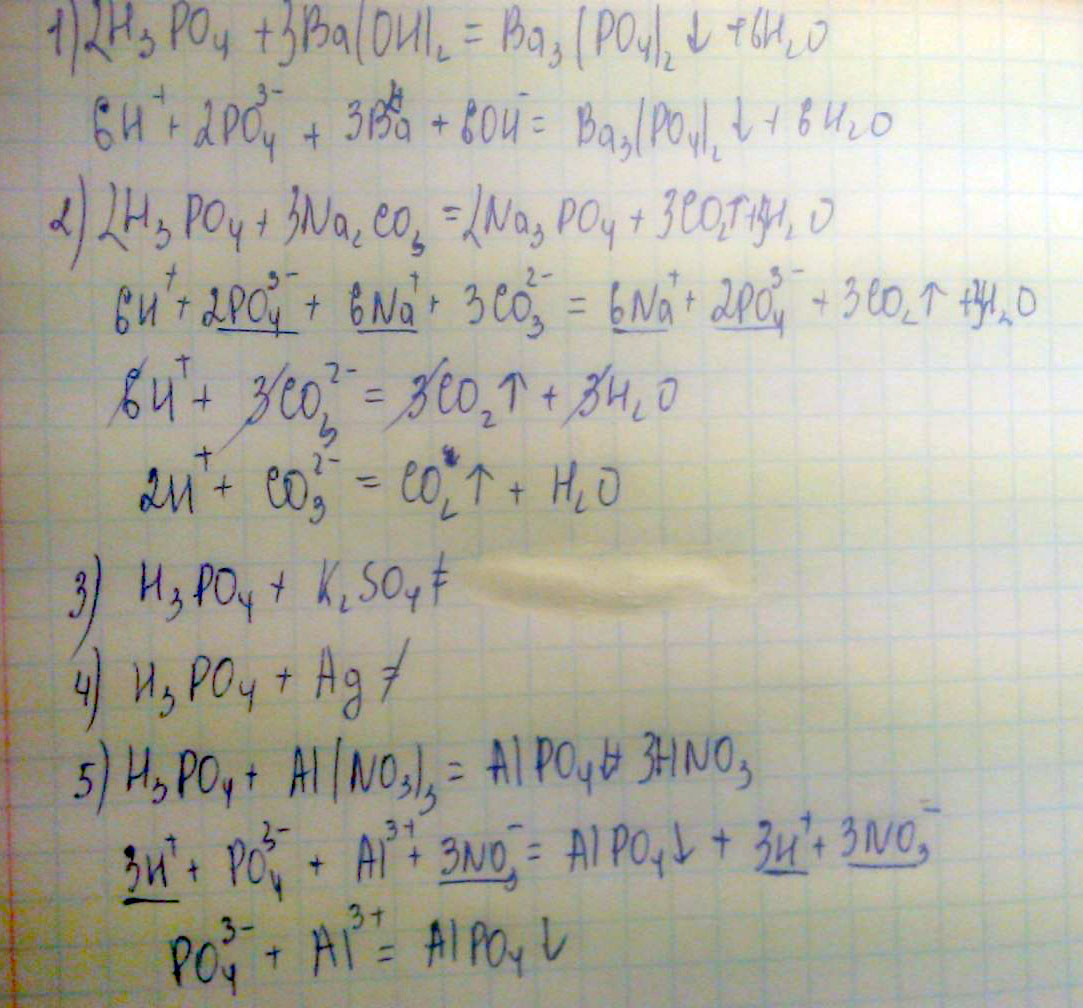
Напишите уравнение реакций в молекулярном и ионном видах:
ZnSO4+K2S =
CuCl2+Ba(OH)2=
