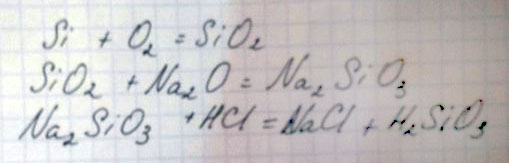Fe(SO4)3-Fe(OH)3-Fe2O3 осуществить превращение
Fe2(SO4)3 + 6NaOH = 2Fe(OH)3 + 3Na2SO4
2Fe(OH)3 + t = Fe2O3 + 3H2O
₁ ₂
Fe₂(SO₄)₃ → 2Fe(OH)₃ → Fe₂O₃
1. Fe₂(SO₄)₃ + 6KOH = 2Fe(OH)₃ + 3K₂SO₄
t
2. 2Fe(OH)₃ = Fe₂O₃ + H₂O
Fe2(SO4)3 + 6NaOH = 2Fe(OH)3 + 3Na2SO4
2Fe(OH)3 + t = Fe2O3 + 3H2O
₁ ₂
Fe₂(SO₄)₃ → 2Fe(OH)₃ → Fe₂O₃
1. Fe₂(SO₄)₃ + 6KOH = 2Fe(OH)₃ + 3K₂SO₄
t
2. 2Fe(OH)₃ = Fe₂O₃ + H₂O
4Al+3O2 = 2Al2O3 соединение (оксид алюминия
3H2SO4+Al2O3 = Al2(SO4)3+3H2O обмен (сульфат алюминия
Al2(SO4)3+6HCl = 2AlCl3+3H2SO4 обмен (хлорид алюминия
AlCl3+3KOH = Al(OH)3+3KCl обмен (гидрооксид алюминия
2Al(OH)3 = Al2O3+3H2O разложение (оксид алюминия
1) C2H6 -> C2H4 + H2 (Над стрелочкой Pt, t)
2) СН2 = СН2 + Н2О -> СН3-СН2-ОН (при t)
3) C2H5OH + HCl -> C2H5Cl + H2O
4) 2C2H5Cl+ 2Na -> C4H10 + 2NaCl
5) C4H10 -> C4H8 + H2
6) C4H8 + HCl -> C4H9Cl
7) 2C4H9CI + 2Na -> C8H18 + 2NaCI
1) MgCO₃ -t-> MgO + CO₂
MgO + 2HNO₃ -> Mg(NO₃)₂ + H₂O
Mg(NO₃)₂ + 2KOH-> Mg(OH)₂ + 2KNO₃
Mg(OH)₂ -t-> MgO + H₂O
2) K₂SiO₃ + 2HCl -> H₂SiO₃ + 2KCl
H₃SiO₃ -t-> H₂O + SiO₂
H₂O + SO₃ -> H₂SO₄
3H₂SO₄ + Al₂O₃ -> Al₂(SO₄)₃ + 3H₂O
Al₂(SO₄)₃ + 6KOH -> 2Al(OH)₃ + 3K₂SO₄
3) MgO + H₂SO₄-> MgSO₄ + H₂O
MgSO₄ + 2NaOH-> Mg(OH)₂+ Na₂SO₄
Mg(OH)₂-t-> MgO + H₂O
1) Si→SiO2→Na2SiO3→H2SiO3
Si + O2 + t = SiO2
SiO2 + 2NaOH + t = Na2SiO3 + H2O
Na2SiO3 + CO2 + H2O = Na2CO3 + H2SiO3
2) Al(OH)3→Al(NO3)3→Al2O3→AlCl3
Al(OH)3 + 3HNO3 = Al(NO3)3 + 3H2O
4Al(NO3)3 + t = 2Al2O3 + 12NO2 + 3O2
Al2O3 + 6HCl = 2AlCl3 + 3H2O
1) задание.
1 реакция:
Si+O2 = SiO2 - р. Соединения.
2 реакция:
2SiO2+2NaOH = 2Na2(SiO3)+H2 - р. Замещения
3 реакция:
Na2SiO3+H2O = H2SiO3+Na2O - р. Замещения