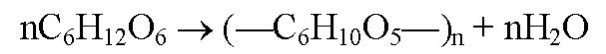Напишите реакцию - задачи и примеры
Почему этен, пропен, бутен используют для получения полимеров, а алканы сами по себе нет?
Напишите реакцию полимеризации
Не используют, так как алканы не вступают в реакцию полимеризации - у них нет кратных связей, которые можно разорвать.
Реакция полимеризации для бутена:
nCH2 = CH-CH2-CH3 = (-CH2-CH2-CH2-) n
Напишите реакцию галогенирования, замещения CH2 = CH-C (CH3)=CH3
(3-метил-бутадиен-1,3)
Бутан имеет два изомера:
1. Н-бутанCH3–CH2–CH2–CH3
2. ИзобутанCH(CH3)3
А. Галогенирование алканов протекает по радикальному механизму. Для инициирования реакции необходимо смесь алкана и галогена облучить УФ-светом или нагреть.
1. CH3–CH2–CH2–CH3 + 6Cl2 = Cl3C–CH2–CH2–CCl3+ 6HCl
2. CH(CH3)3 + 9Cl2 = CH(CCl3)3 + 9HCl
Б. Алканы реагируют с 10 % раствором азотной кислоты или оксидом азота NO2 в газовой фазе при температуре 140 °C и небольшом давлении с образованием нитропроизводных. В результате реакции образуются смеси продуктов. RH + HNO3 = RNO2 + H2O.
1. CH3–CH2–CH2–CH3 + 2HNO3 = О2NН2C–CH2–CH2–CН2NO2 + 2H2O.
2. CH(CH3)3 + 3HNO3 = CH(CH2NO2)3 + 3H2O.
При сплавлении 16,4 натриевой соли предельной одноосновной карбоновой кислоты с избытком едкого натра выделилось 4,48 л
1) запишите молекулярную формулу исходного вещества
4 ) напишите реакцию соли с бромметаном
СnH₂n+₁COONa + NaOH -> СnH₂n+₂ + Na₂CO₃; ню(СnH₂n+₁COONa )= ню(СnH₂n+₂) =4,48/22,4 = 0,2 моль; M(СnH₂n+₁COONa )= 16,4/0,2 = 82 г/моль; 14n +1 + 12 + 32 + 23 = 82; 14n =14; n = 1. CH₃COONa; C₂H₃O₂Na; CH₃COONa + CH₃Br ->CH₃COOCH₃ + NaBr
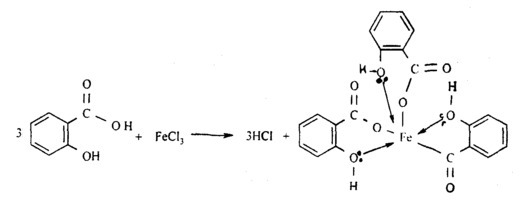
Напишите реакцию салициловой кислоты с хлоридом железа(III)
В результате реакции получается хелатный комплекс железа:
Напишите реакцию поликонденсации. Дайте определение
Реакция поликонденсации - это процесс образования высокомолекулярных веществ из низкомолекулярных, идущий с выделением побочных продуктов. В отличие от реакции полимеризации этот процесс не может быть отнесен к типу реакций соединения.
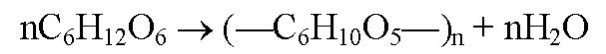
Напишите реакцию взаимодействия бериллия с водным раствором едкого натра.
Сумма всех коэффициентов в уравнении равна
Укажите формулу восстановителя
Укажите молекулу окислителя
Напишите формулу бериллийсодержащего продукта
К какому классу соединений принадлежит бериллийсодержащий продукт?
основания
кислоты
оксиды
средние соли
кислые соли
основные соли
комплексные соли
Назовите бериллийсодержащий продукт по международной номенклатуре
Какой бериллийсодержащий продукт образуется при СПЛАВЛЕНИИ бериллия с гидроксидом натрия?
Be + 2NaOH + 2H2O → Na2[Be(OH)4] + H2
Сумма всех коэффициентов в уравнении равна 7. Восстановитель - Beокислитель - NaOH
Na2[Be(OH)4] - комплексная сольтетрагидроксобериллата(II) натрия
Be + 2NaOH → Na2BeO2 + H2 при сплавлении
Напишите реакцию получения бутилового эфира гексановой кислоты
СН₃-(СН₂)₂-СН₂-ОН + НООС-(СН₂)₄-СН₃ =
Н₂О +СН₃-(СН₂)₂-СН₂-О-С(О-(СН₂)₄-СН₃
В формуле эфира там, где кислород в скобках стоит, проведите от углерода, при котором кислород в скобках, двойную связь вверх или вниз.
Впрочем. И так можно.
Напишите реакцию хим. уравнений между:
А) Оксидом купрума и сульфатной кислотой
Б) Оксидом Алюминия и хлоридной кислотой
В) оксидом натрия и хлоридной кислотой
Г) магнием и сульфатной кислотой
Д) Кальцием и хлоридной кислотой
,
А CuO + H₂SO₄ = CuSO₄ + H₂O-сульфат меди (II) и вода
б Al₂O₃ + 6HCl = 2AlCl₃ + 3H₂O - хлорид алюминия и вода
в Na₂O + 2HCl = 2NaCl + H₂O - хлорид натрия и вода
г Mg + H₂SO₄ = MgSO₄ + H₂ - сульфат магния и водород
д Ca + 2HCl = CaCl₂ + H₂ - хлорид кальция и водород
Напишите реакцию получения фенетола (этиловый эфир фенола из бензола.
Реакция здесь не одна.
Один из способов - то, что в предыдущем ответе (две стадии.
С6Н6 + Cl2 => кат. =>C6H5Cl + HCl
C6H5Cl + NaOH =>t,p=>C6H5OH + NaCl
Этот способ оказывается дорогим, экономически нецелесообразным.
Во всем мире фенол из бензола получают по-другому:
1) бензол + пропилен (пропен =[катализатор AlCl3] = кумол (изопропилбензол
2) кумол окисляют кислородом в присутствии серной кислоты - получают фенол и ацетон.
1) Электронная формула атома натрия.
2) Какое вещество обладает наиболее ярко выраженными металлическими свойствами:
a) Алюминий, б Кремний, в Магний, г Натрий
3) Какое вещество наиболее энергично реагирует с водой, напишите реакцию:
а Калий, б Литий, в Рубидий.
4) Выберите ряд в котором все вещества реагируют с кальцием, также подкрепите уравнения реакций:
а CO₂ HCl H₂
б Cl₂ H₂O H₂SO₄
в NaOH H₂O HCl
г S H₂SO₄ SO₃
5) Рассчитайте массу металла, который можно получить из 160г оксида меди.
6) Предложите три способа получение сульфата железа (II). Ответ подтвердите уравнение реакций.
Что можете, сделайте, . (Можете без уравнений некоторые номера делать (4 или 6)).
1) 1s^2 2s^2 2p^6 3s^1 (если нужно, могу нарисовать строение
2) Это натрий. Т. К Ме свойства убывают в периодах.
3) Калий. 2K+2H2O = 2KOH+H2 (газ
5) Ур. Реакции 2CuO = 2Cu+O2
Масса CuO = масса/молярн. = 160/180 = 2 моль
По уравнению видим, что меди тоже 2 моль.
Масса меди = 2*64 = 128 (64 - молярная масса меди