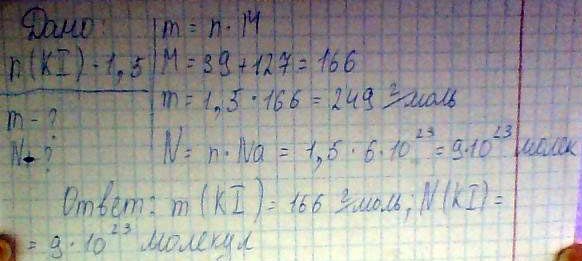Найти число молекул - задачи и примеры
1) Найдите массу простого вещества серы (S) если его количество составляет 2,5 моль
2) Сколько молекул и какой обьём содержится в 14 г. Угарного раза СО?
3) Найдите обьём озона 0(3 маленькая ) число молекул которого составляет 24 * 10/23
1) m = nM
M (S) = 32 г/моль
m = 2*32 = 64 г
2) V = n * Vm, где Vm = 22,4 дм³ (устойчивая величина)
N = Nа*n, где Na = 6,02 * 10 в 23 степени (устойчивая величина)
n = m/M
M (CO) = 12 + 16 = 28 г/моль
n (CO) = 14/28 = 0,2 моль
V (CO) = 0,2*22,4 = 4,48 дм³
N = 0,2*6,02*10 в 23 степени = 1,204 * 10 в 23 степени молекул
3) V = n * Vm, где Vm = 22,4 (устойчивая величина)
N = Nа*n, где Na = 6,02 * 10 в 23 степени (устойчивая величина)
Отсюда n = N/Na
n(озона) = 24 *10 в 23 степени / 6,02 * 10 в 23 степени = 3,99 моль = 4 моль
V(озона) = 4 * 22,4 = 89,6 дм³
1.Mr(MnO2)
2. Вычислите массу, объем, число молекул 0,5 моль метана
дано:
n(CH₄) = 0,5 моль
Найти:m(CH₄), V(CH₄), N(CH₄)
Решение:
M(CH₄) = 12 + 1·4 = 16 гмоль
m(CH₄) = n·M = 0,5 моль · 16гмоль = 8 г
V(CH₄) = Vm·n = 22,4 лмоль · 0,5 моль = 11,2 л
N(CH₄) = n·Na = 0,5 моль · 6,023 ·10²³ моль⁻¹ = 3 · 10²³ молекул
Ответ: m(CH₄) = 8 г, V(CH₄) = 11,2 л,N(CH₄)= 3 · 10²³ молекул
Mr(MnO₂) = 55 + 16·2 = 87
1.Mr(MnO2) = 55+16*2 = 87г/моль
2. Масса m(CH4)=n*M = 0.5 моль*16г/моль=8 г
1) найдите массу 67.2м серной кислоты, приормальных условиях
2) найдите массу и число молекул 5.6 азота
3) найдитте массу и число молекул 22.4 л гидроксита натрия
1) V(H2SO4)= 67,2 м3
m = nM
n = V/Vm
m = V/Vm*M
m(H2SO4)=67,2/22,4*98 = 294кг
2) V(N2)=5,6 м3
m = nM=V/Vm*M
N = nNA=V/Vm*NA
m(N2)=5,6/22,4*28 = 7 кг
N(N2)=5,6/22,4*6*10^23 = 1,5*10^23
3) V(NaOH)=22,4л
m = nM=V/Vm*M
N = nNA=V/Vm*NA
m(NaOH)=22,4/22,4*40 = 40г
N(NaOH)=22,4/22,4*6*10^23 = 6*10^23
1. Рассчитайте массу и число молекул соединений, взятых количеством вещества: а 2 моль AlCl3 б 0,84 моль K2CO3
2. Какому количеству вещества соответствует:
а 100 г Fe2(SO4)3
б 88 г N2O
в 0,3 * 10 в 24 степени атомов Zn
1.
аn(AlCl3)=2 моль
m = n*M
N = n*NA
m(AlCl3)=2*133,5 = 267 г
N(AlCl3)=2*6*10^23 = 18*10^24 молекул
бn(K2CO3)=0,84 моль
m = n*M
N = n*NA
m(K2CO3)=0,84*138 = 115,92 г
N(K2CO3)=0,84*6*10^23 = 5,04*10^23 молекул
2.
аm(Fe2(SO4)3)=100г
n = m/M
n(Fe2(SO4)3)=100/400 = 0,25 моль
бm(N2O)= 88г
n = m/M
n(N2O)=88/44 = 2 моль
вN(Zn)=0,3*10^24
n = N/NA
n(Zn)=0,3*10^24/6*10^23 = 0,5 моль
Определите массу и число молекул в иодиде калия количеством вещества 1,5 моль
N(KI) = 1,5 моль
m(KI) -
N(KI) -
Решение
m(KI) = n*M = 1,5 моль * 166 г/моль = 249 г
N(KI) = n * N(A) = 1,5 * 6 * 10^23 = 9 * 10^23
Вот.
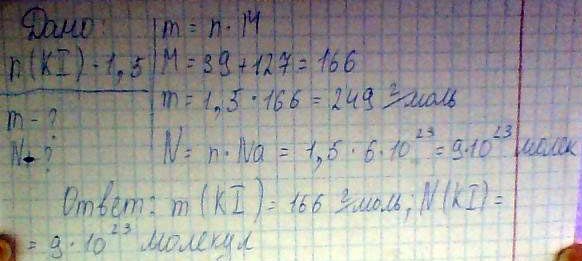
1. Определите число молекул, содержащихся в 7 молях водорода.
Главное для решение этой задачи - знать, что в одном моле любого вещества содержится 6*10^23 молекул вещества.
Молекулярный вес водорода равен 2.
Масса одной молекулы водорода равна 2/число Авогадро, то есть 2/(6*10^23) = 3.33*10^-24
Число молей в 600 г водорода равно 600/2 = 300
число молекул 300 * 6*10^23 = 1,8 * 10^26 2 Нравится Пожаловаться
Дано:
V(H2) = 0.2 моль
N(H2) -
Решение:
V = N/NA
N = VNA
N = 0.2 моль x 6.02x10(23степени = 1.2 х 10(23степени