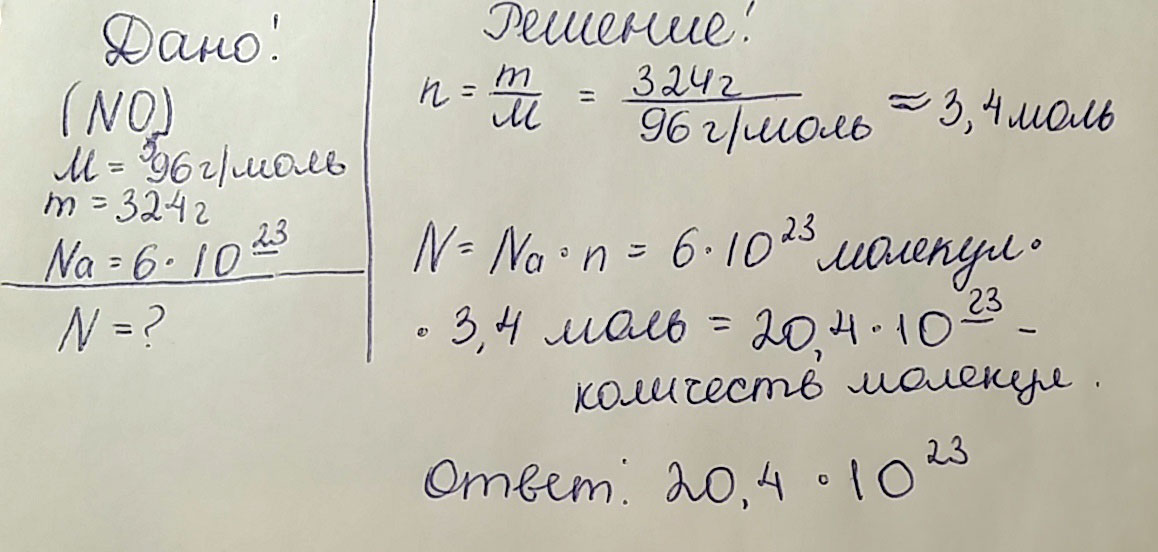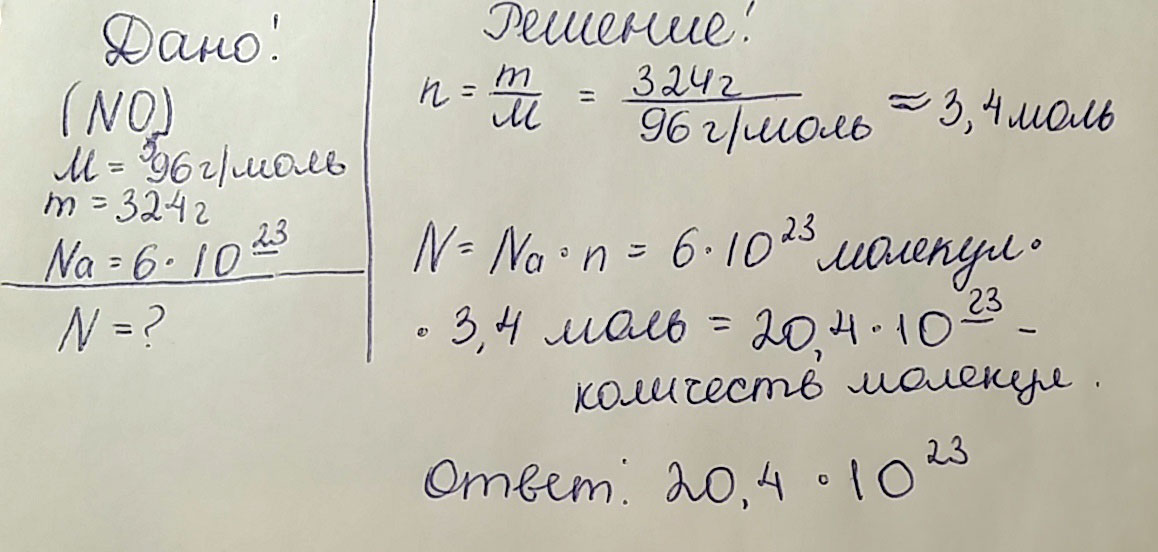Найти число молекул - задачи и примеры
Найдите число молекул серной кислоты, которое содержится в 70 г её 20% раствора.
В 1 молекуле серной кислоты 4 атома кислорода. В одной молекуле воды - 1 атом кислорода. Водорода в кислоте - 2 атома, в воде - тоже 2.
Если обозначить число молекул кислоты за Х, а воды - за У, то
4х+у = 2х+2у.
Упрощая, получим у=2х. Иными словами, воды в растворе в 2 раза больше, чем кислоты (по количеству вещества.
Если кислоты 1 моль (98 г, то воды 2 моль (18*2 = 36 г.
Массовая доля кислоты 98/(98+36)=0,731, или в процентах 73,1
Дальше. Если этого раствора 100 г, то кислотыв нем 100*0,731 = 73,1 г.
Если это составляет 30%, то масса всего раствора 73,1/30*100 = 243,7 г.
А объем получим, если теперь эту массу разделим на плотность
243,7/1,22 = 199,8 мл.
M(H2SO4) = m*ω = 70 * 0.2 = 14г
n = m/M = 14/98 = 0.143моль
n = N/NАвогадро ==> N = n*NАвогадро = 0.143 * 6.022 * 10²³ = 0,861146*10²³
Определить число молекул и атомов в хлоре а количеством вещества 7 моль б массой 7,1г.
Формула-Cl2
из формулы видно:
n(Cl)=2n(Cl2)
Cl-атом
Cl2-молекула
N.A(A в индексе = 6,023*10^23
N.A-это число Авогадра ( постоянный
а
n(Cl2)=7моль
n(Cl)=2*7 = 14моль
N(Cl2)=n(Cl2)*N.A =
=7*6,023*10^23 = 4.216*10^24
N(Cl)=n(Cl)*N.A =
=14*6*10^23 = 8.4322*10^23
б
M(Cl2)=2*35,5 = 71г/моль
n(Cl2)=m/M = 7.1/71 = 0,1моль
n(Cl)=0,1*2 = 0,2моль
N(Cl2)=n(Cl2)*N.A)=
=0,1*6,023*10^23 = 6,023*10^22
N(Cl)=n(Cl)*N.A =
=0,1*6,023*10^23 = 1,2046*10^23
1. Закончите предложение
1) Химическая связь между атомами элементов, имеющих разную электроотрицательность, называется
2) Связь между частично положительными атомами водорода одной молекулы и частично отрицательными атомами кислорода другой молекулы называется
3) Правильное, строго упорядоченное распоряжение частиц вещества в пространстве, называется
4) Кристаллическая решетка, в узлах которой расположены молекулы, называется
5) Кристаллическая решетка, в узлах которой атомы, называется
2. Рассчитайте массовую долю алюминия в следующих веществах
1) Al2O3
2) AlCl3
3) Al(NO3)3
3. Какой объем пр нормальных условиях занимают
1)3 моль любого газа
2) m(O2)=13 г
4. Рассчитайте число молекул (N) вещества в данной массе m:
1)(BaSO4)=115 г
2)(AgNO3)=12 г
5. Вычислите среднюю скорость реакции N2+H2 = 2NH3, если начальная концентрация N2 составляла 0,90 моль/л, а H2-1,10 моль/л. Спустя 15 с концентрация N2 снизилась до 0,83 моль/л. Определите среднюю скорость реакции и концентрацию H2 в этот момент времени
6. Классифицируйте и назовите следующие соли
1) MnOHNO3
2) BaSO4
3) NaHCO3
4) BiOHSO3
5) Ca(HS)2
1. 1) такая связь называется ионной
4. 1) N = Na • ню; от сюда находим ню по формуле: данная масса/на молярную массу вещества (BaSO4) от сюда находим N= 2.97•10в 23 степени
Так же находим число молекул следующего вещества (AgNO3) и оно равно 0.43•10в 23 степени
1. В ложке воды содержится около 0,5 моль вещества. Вычислите число молекул воды в ложке.
Дано:
n (H₂O) = 0,5 моль.
Найти:
N (H₂O) —?
Решение:
N = Nₐ · n;
Nₐ = 6 · 10²³ молекул/моль.
N (H₂O) = 6 · 10²³ молекул/моль · 0,5 моль = 3 · 10²³ (молекул.
Ответ: 3 · 10²³ молекул.
Найти число молекул и объём 128мне SO2
128 граммов SO2 - это 2 моль, значит это 1,2х 10 в 24 степени молекул и при н.у. Объем 44,8 литра.
M = 128 (г)
n = m/M
M(SO2)=32+2*16 = 64(г)/моль
n = 128/64 = 2(моль
N = Na*n, где Na - число Авагадро = 6.02*10^23 (г)/моль
N = 6.02*10^23*2 = 12.04*10^23(молекул
V = Vm*n, где Vm- объем газа при н.у. = 22.4 (л)/моль
V = 22.4*2 = 44.8 (л)
Определите число молекул оксида азота (V) массой 324 грамма
Вот. Первым делом необходимо найти количество вещества, а потом уже умножать это число на число Авагадро