Степень окисления элементов в соединении Li2CO3
H202
N2O
K2CrO4
SO2
Li₂CO₃:
Li⁺
C⁺⁴
O⁻²
H₂O₂:
H⁺
O⁻
N₂O:
N⁺
O⁻²
K2CrO₄:
K⁺
Cr⁺⁶
O⁻²
SO₂:
S⁺⁴
O⁻²
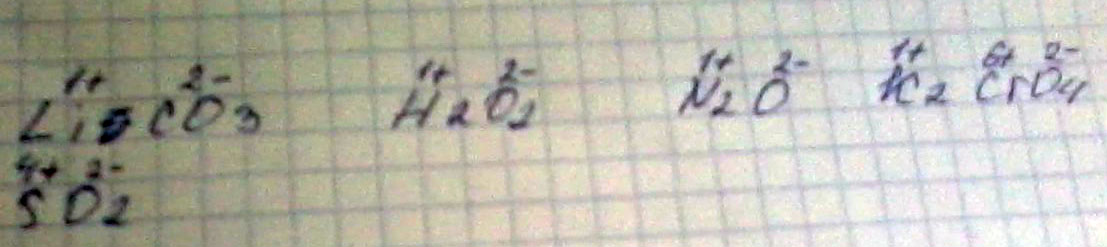
Степень окисления элементов главной подгруппы 5 группы в соединениях с металлами и водородом равна ?
NH3 - аммиак
Mg3N2 - нитрид магния
Степень окисления (-3)
-3, т. к. стоят в V группе им не хватает 3 электронов. Просто вспомни аммиак и фосфин, которые проходят по школьной программе.
1) Укажите степень окисления элементов в веществах, формулы которых: H3PO4, Fe(OH)2. Запишите соответствующие им оксиды. Назовите вещества.
2) Составьте формулы солей, состоящих из: - кислотного остатка серной кислоты и следующих металлов: - Натрия, Магния, Алюминия.
3) Рассчитай массу сульфата калия и воды, которые надо взять для приготовления 60г раствора с массовой долей сульфата калия 15%
4) Из перечисленных формул выпишите отдельно формулы оксидов, оснований, кислот, солей и дайте им названия: Na2O, CuSO4, HNO2, Fe(OH)3, K2SO4, KOH, HNO3, SO3.
1) H₃⁺¹P⁺⁵O₄⁻² = P₂O₅
Fe⁺²(O⁻²H⁺¹)₂⁻ = FeO
2)
Na₂SO₄, MgSO₄, Al₂(SO₄)₃
3)
m(K₂SO₄) = 60 г*0,15 = 9 г
m(H₂O) = 60 - 9 = 51 g
4)
Оксиды
Na₂O - оксид натрия (основный)
SO₃ - оксид серы (VI) (кислотный)
Основания:
Fe(OH)₃ - гидроксид железа (III) - нерастворимое основание
KOH - гидроксид калия - щелочь
Кислоты:
HNO₂ - азотистая кислородсодержащая кислота
HNO₃ - азотная кислородсодержащая кислота
CuSO₄ - сульфат меди (II) - средняя соль
K₂SO₄ - сульфат калия - средняя соль
Степень окисления элементов в вещесьвах SIH3 K3N ALCL3 CR2O7 NI2S3
-3 + + -3 +3 - +7 -2 +3 -2
Si H3; K3N; Al Cl3; Cr2O7; Ni2S3 Немного сместились степени окисления, смотри фото
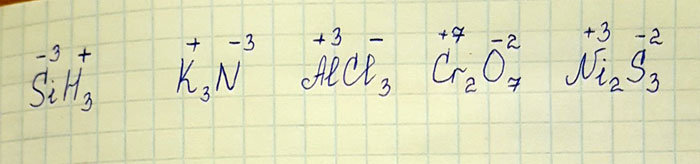
Составьте уравнение реакции серы: а кислородом, б водородом, в натрием. Добавить вид химической связи в каждой из соединений. Расставьте степени окисления элементов, проанализируйте, как изменяется степень окисления элементов при химических реакций.
АS+O2 = SO2(ковалентная полярная связь, степень окисления серы +4)
бH2+S = H2S(ковалентная полярная связь, Степень окисления серы -2)
в2Na+S = Na2S (ионная, степень окисления -2)