Смесь карбонатов натрия и кальция масссой 77,4 г прокалили. Масса смеси после прокаливания составила 62 г. Определите массовые доли компонентов в исходной смеси
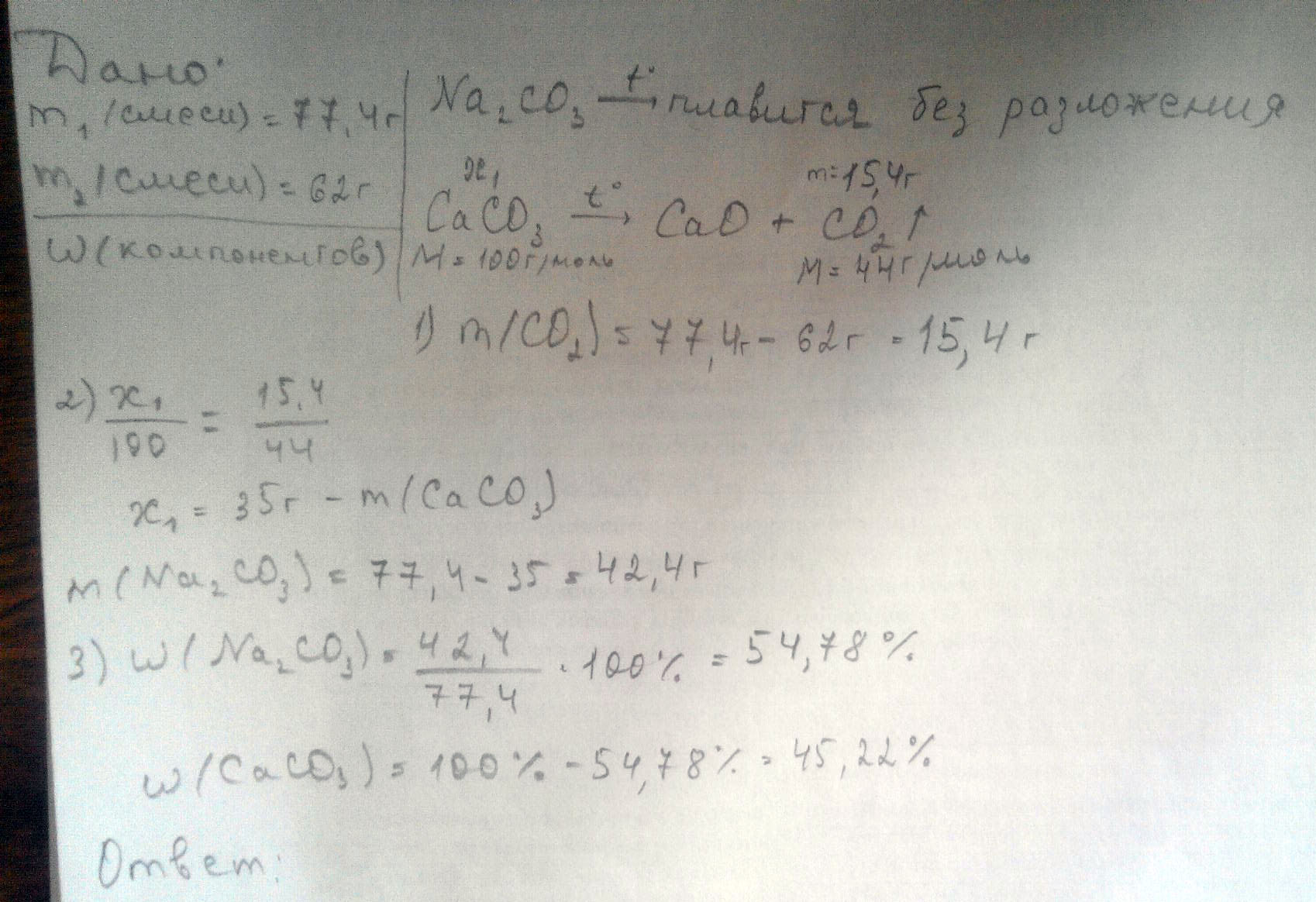
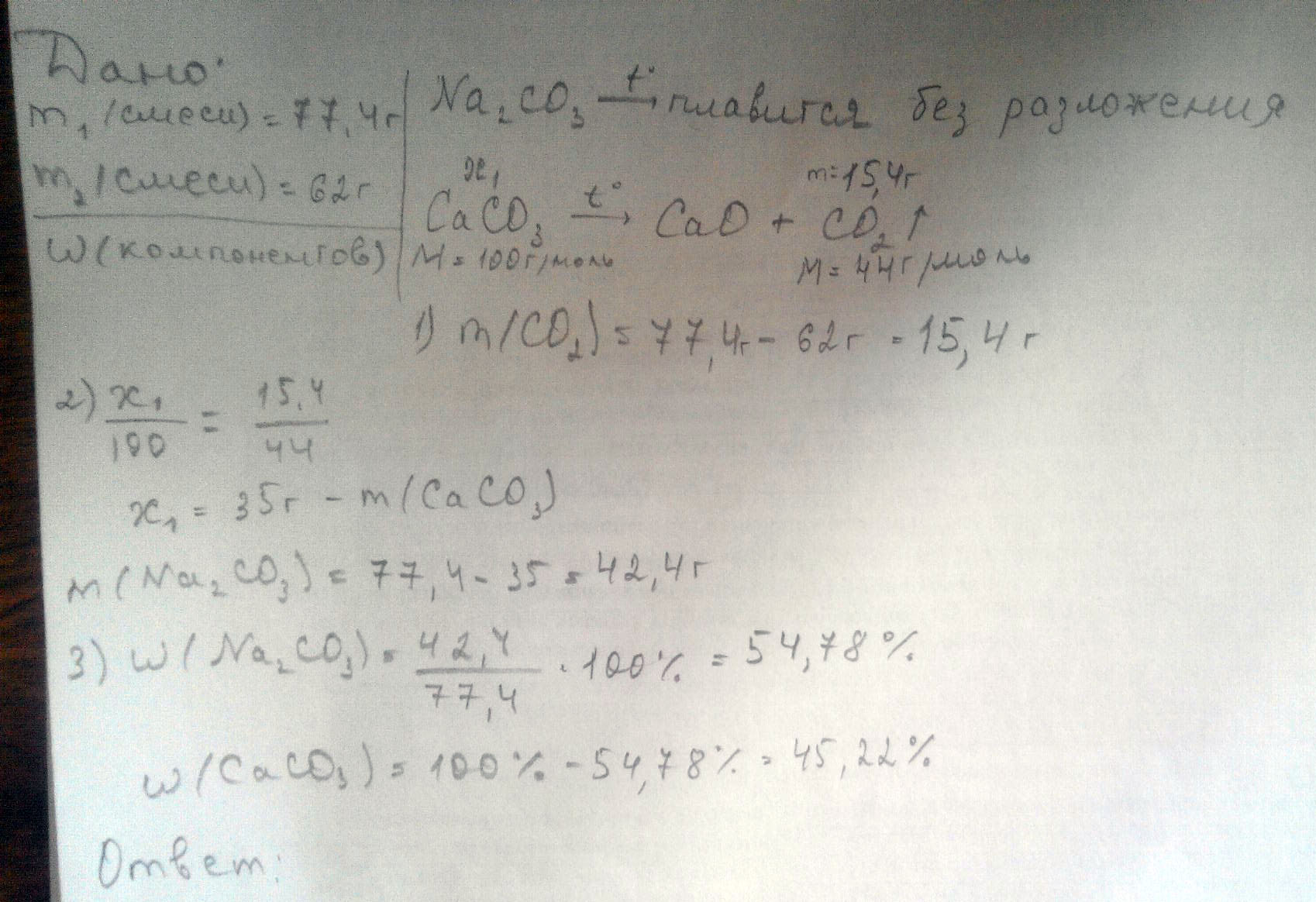
Это пропен и циклопропан: CH₂=CH-CH₃ + Br₂ ->Br-CH₂-CHBr-CH₃; Δ + Br₂ ->Br-CH₂-CH₂-CH₂-Br; т. к. Это изомеры, то массовые доли равны объемным и равны мольным Массовые доли соотносятся как 2 : 3. Значит в смеси 40% пропена и 60% циклопропана
Дано
m(см = 10г
W(NaCl)=30%
W(KCl)=70%
найти
Nсмеси-
Находим массу NaCl и KCl
Пусть 100% - 10г
Тогда 30% - ХГ х=3г NaCl
100%-10g
70%-Xg X = 7g KCl
определяем молекулярные массы NaCl и KCl
M(NaCl)=23+35.5 =58.5g/mol
M(KCl)=39+35.5 = 74.5g/mol
зная массы и молекулярные массы находим молярные массы NaCl и KCl
ню = m/M
ню(NaCl)=3/58.5 = 0.05 mol
ню(KCl) = 7/74.5 = 0.09 mol
общее количество молей в газе равно 0.05+0.09 = 0.14 моль
Определяем количество молекул в 10 гр. В смеси
по формуле N = ню*Na
гдеNa = 6.02*10^23
N = 0.14*6.02*10^23 = 0.84*10^23
Зная что 1г содержится 0.84*10^23
а в 10г - Хгр
Х = 10*0.84*10^23 X = 8.4*10^23 молекул
Ответ 8.4*10^23 молекул
При нагревании разложился только гидрокарбонат натрия.
2NaHCO3 = Na2CO3+H2O+CO2
M(NaHCO3)=84г/моль
М(H2O и CO2)=18+44 = 62г/моль
Смесь стала легче за счёт удаления воды и углекислого газа.
Ушло 96г-69г = 27г
Составим пропорцию по уравнению реакции и узнаем, сколько гидрокарбоната надо разложить, чтобы выделилось 27г воды и углекислого газа.
из ХгNaHCO3 выделится 27г
а из 168г/моль - 62 г/моль
Х = 73г
Значит исходная смесь содержала 73гNaHCO3, и 96-73 = 23г Na2CO3
Записываем уравнение первой реакции CaCl2+Na2CO3 = CaCO3+2NaCL Найдем массу осадка CaCO3 для этого составим пропорцию. М(CaCL2)=111. M(CaCO3)=100 Из 111г. СaCl2 можно получить 100г CaCO3. Из х г. CaCl2-неизвестно. m(CaCO3)=100x/111 = 0.9x. Записываем второе уравнение Сa(NO3)2+Na2CO3 = CaCO3+2NaNO3. m(Ca(NO3)2 = 13,7-x. M(Ca(NO3)2)=164. M(CaCO3)=100 Из 164г. Ca(NO3)2 = 100г CaCO3 Из 13,7-x г. Ca(NO3)2 = неизвестно CaCO3 m(CaCO3)=(13,7-x)*100/164 = 8,354-0,61x. Составляем уравнение m(CaCO3)=0,9x+8,354-0,61x = 10 8,354+0,29x = 10 0,29x = 1,646 x = 5,676г. Массовая доля хлорида = 5,676/13,7 = 41,4% Массовая доля нитрата = 58,6%
Примем массу хлорида кальция m(CaCl2) = х г, а массу образующегося при этом СаСО3 - m(CaCO3) = у г; и соответственно m(Ca(NO3)2) = (13,7-х г, а m(CaCO3) = (10-у г
х г у г
СaCl2 + Na2CO3 = CaCO3 + 2NaCl
111 г 100 г
(13.7-х г (10-у г
Сa(NO3)2 + Na2CO3 = CaCO3 + 2NaNO3
164 г 100 г
Составляем систему двух уравнений:
100х=111у
1370-100х=1640-164у
Решив систему, получим, что
х=5,654 или m(CaCl2) = 5.654 г
m(Ca(NO3)2) = 13.7 г - 5,654 г = 8,046 г
ω(СaCl2) = 5.654/13,7×100% = 41,27%
ω(Сa(NO3)2) = 8,046/13,7×100% = 58,73%
Если равние массовые доли кислот, значит, равные и массы газов в смеси. Пусть масса каждого газа = 100 г.
V(HCl) = m/M*22.4 = 100/36.5*22.4 = 61.37 л
V(HBr) = 100/81*22.4 = 27.65 л
V(смеси = 27,65+6137 = 89,02 л
Ф (НС1) = 61,37/89,02*100 = 69%
Ф(НВг = 27,65/89,02*100 = 31%