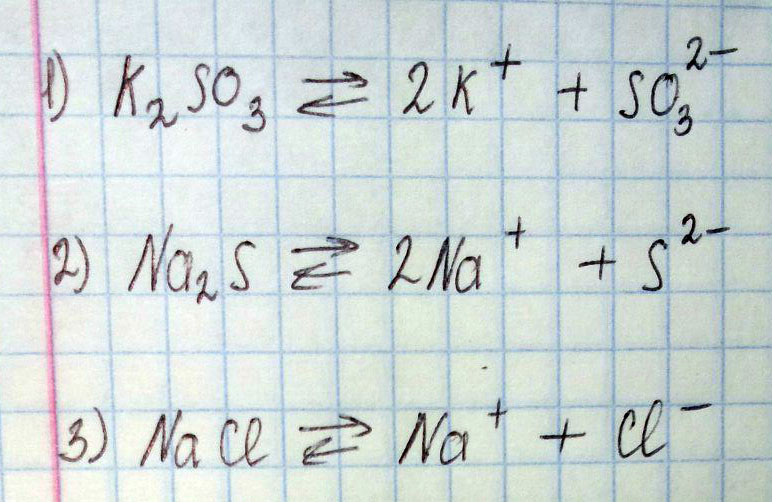Реакции диссоциации - задачи и примеры
Составьте уравнения электролитической диссоциации веществ CuCl2; KMnO4; NaBr; Ca(OH)2; Fe(No3)3; Na3PO4; Al2(SO4)3; AgNO3; ZnSO4; AlCl3; Mg(NO3)².
CuCl2 → Cu²⁺ + 2Cl⁻
KMnO4 → K⁺ + MnO4⁻
NaBr → Na⁺ + Br⁻
Ca(OH)2 → Ca⁺ + 2OH⁻
Fe(NO3)3 → Fe³⁺ + 3NO3⁻
Na3PO4 = 3Na⁺ + PO4³⁻
Al2(SO4)3 → 2Al³⁺ + 3SO4²⁻
AgNO3 → Ag⁺ + NO3⁻
ZnSO4 → Zn²⁺ + SO4²⁻
AlCl3 = Al³⁺ + 3Cl⁻
Mg(NO3)2 → Mg²⁺ + 2NO3⁻
Напишите уравнения электролитической диссоциации: аK3[Fe(CN)6]
б [Ag(NH3)2]CL.
в Н2[SiCl6]. Напишите, только по подробней
Первая схема будет диссоциация на внешнюю и внутреннюю сферы
Вторая схема будет диссоциация внутренней сферы
а $$ \begin{array}{l} \mathrm{H_{2}[SiCl_{6}] \leftrightarrows 2H^{+} + [SiCl_{6}]^{2-}} \mathrm{[SiCl_{6}]^{2-} \leftrightarrows Si^{4+} + 6Cl^{-}} \end{array} $$
Вещества, образующие при диссоциации в качестве катионов только ионы водорода, являются
1) основаниями
2) щелочами
3) кислыми солями
4) кислотами
Кислотами конечно же
пример:HCl = H(+)+Cl(-)
катион водорода и анион хлора
Они являются кислотами т.к при диссоциации кислоты разлагаются на катионы водорода и онионы кислотных остатков
Напишите уравнения электролитической диссоциации следующих веществ:
АH2SO4, HNO3;
БKOH, Ca(OH)2
ВAgNO3, K3PO4, NaSO4.
Какие ионы определяют свойства этих электролитов.
H2SO4->2H^(+) +SO4^2-
HNO3->H^(+) +NO3^(-)
ROH-> K^(+) + OH^(-)
Ca(OH)2-> Ca^(2+) + 2OH^(-)
AgNO3-> Ag^(+) + NO3^(-)
K3PO4->3K^(+) + PO4^(3-)
Na2SO4-> 2Na^(+) + SO4^(2-)
Свойство кислот определяет ион - Н^(+)
Свойство оснований ион - OH^(-)
Напишите уравнения процессов диссоциации следующих соединений K2SO3. Na2S. NaCL.
+1 -2
K2SO3 = 2K+SO3
+1 -2
Na2S = 2Na+S
+1 -1
NaCl = Na+Cl
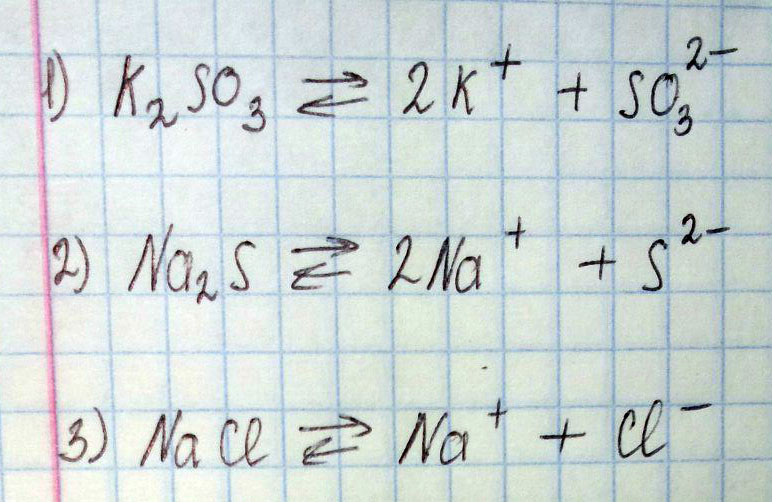
Напишите уравнения электролитической диссоциации BaCl2, Al(OH)3, Ca(NO3)2, H2SO4.
BaCl2 = Ba⁺+2Cl⁻
Гидроксид алюминия - амфотерный гидроксид, нерастворим в воде, диссоциация незначительная, ступенчатая, происходит, главным образом, по первой ступени:
Al(OH)3 = Al(OH)2⁺ +OH⁻
Al(OH)2 + = Al(OH)⁺ + OH⁻
Al(OH)+ = Al3⁺ + OH⁻
Ca(NO₃)2= Ca²⁺+2NO₃⁻
H2SO4 = 2H⁺+SO4²⁻