Какое количество нитрата калия имеет массу 18 грамм
KNO3
m = 18 (г)
n = m/M
M(KNO3)=39+14+3*16 = 101 (г)/моль
n = 18/101 = 0.18 (моль
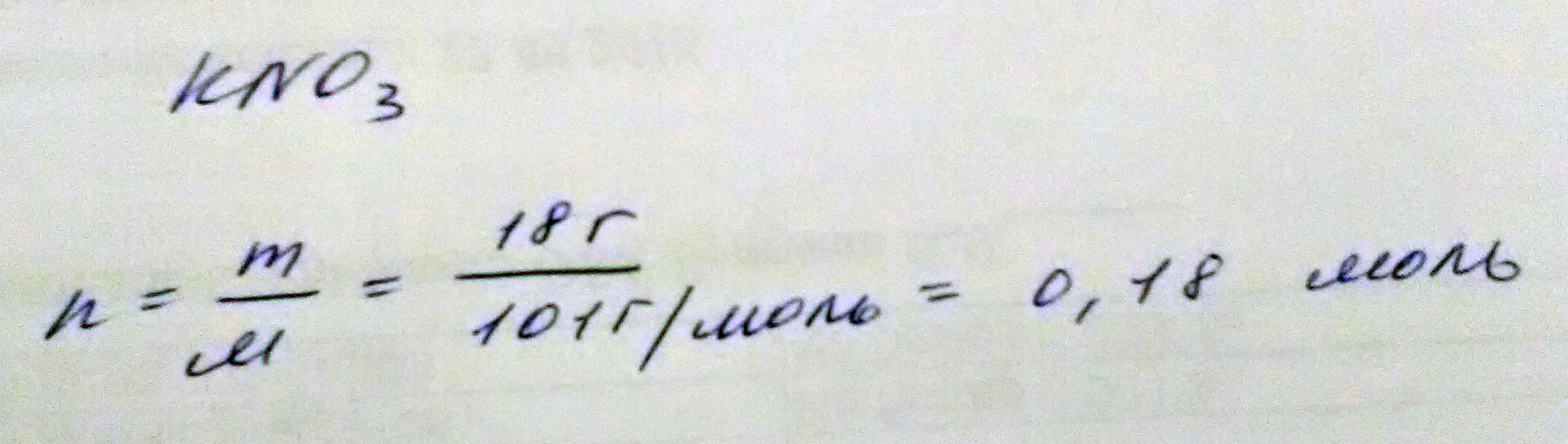
KNO3
m = 18 (г)
n = m/M
M(KNO3)=39+14+3*16 = 101 (г)/моль
n = 18/101 = 0.18 (моль
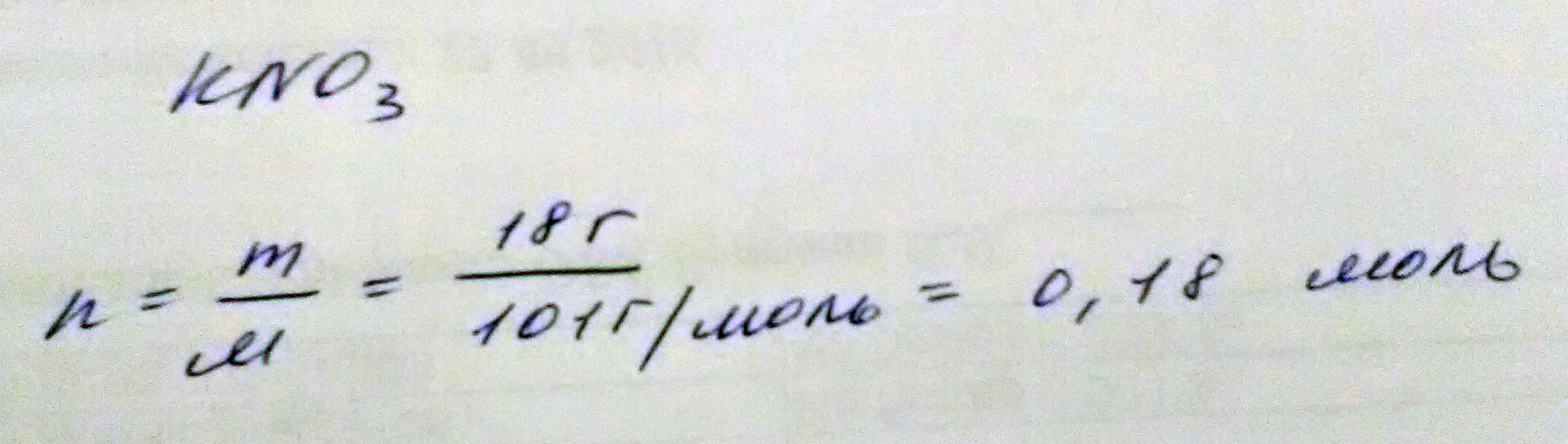
M= 50.8 (г)
n = m/M
M(I2)=2*127 = 254(г)/моль
n = 50.8/254 = 0.2(моль)
N = Na*n, где Na- число Авогадро = 6.02*10^23 (г)/моль
N = 6.02*10^23*0.2 = 1.2*10^23(молекул)
N = 2*10^23 (молекул)
n = N/Na, где Na- число Авогадро = 6.02*10^23 (г)/моль
n = 2*10^23 / 6.02*10^23 = 0.33(моль)
V = Vm*n, где Vm - объем газа при н.у. = 22.4 (л)/моль
V = 22.4*0.33 = 7.39 (л)
1) Mr(Fe2O3)=56*2+16*3 = 160
уравнение:
хгр 20гр
2Fe2O3+3C = 4Fe+3CO2
2*160 4*56
320 224
x-20гр
320гр-224гр
х=320*20/224 = 28,6 гр оксида
10гр хмоль
2) Cu2O+H2 = 2Cu+H2O
64*2+16 1 моль
144 гр
10гр-х
144-1
х=10*1/144 = 0,1иоль воды 1,8 граммв
для приготовления 10%-го раствора соли необходимо взять
1)50 грамм воды и 5 грамм соли
2)50 грамм воды и 10 грамм соли
3)90 грамм воды и 5 грамм соли
4)90 грамм воды и 10 грамм соли
Атомный вес йода равен 127 грамм/моль
Моль. Вес йода вещества так как в молекуле 2 атома I2 = 127*2 = 254 грамм/моль.
Это значит 1 моль йода вещества весит 254 грамма.
У нас 50,8 грамм йода, что составляет 50,8/254 = 0,2 моля.
Значит 50,8 грамм йода это 0,2 моля.
Согласно числа Авогадро мы знаем сколько молекул в 1 моле вещества.
Теперь рассчитаем сколько молекул в 0,2 молях вещества:
молекул.
Ответ: 50,8 грамм йода содержит молекул.
Количество вещества(n) определяется по формуле: n = m(масса, в данном случае NaOH)/M(молярная масса(вычисляется по таблице Менделеева:Na по таблице 23 О по таблице 16 Р по таблице 1, складываем получается М(NaOH)=40, Находим кол-во вещества по формуле:n = m/M подставляем значения: n = 0.4/40 = 0.01-количество вещества NaOH